تعریف سرطان نادر
تعریف درستی برای سرطان نادر وجود ندارد.
در کشورهای اروپایی، بیماری های نادر اغلب به عنوان بیماری هایی با فراوانی کمتر از 50/100000 در سال شناخته می شوند.
مشکل این تعریف این است که مبتنی بر بروز است، که به طور دقیق بار سلامتی رویدادهای بیماری مانند بدخیمی را نشان نمی دهد.
بدخیمیهای نادر معمولاً در گروه بیماریهای نادر دستهبندی میشوند که در اتحادیه اروپا به عنوان بیماریهایی با فراوانی کمتر از پنج مورد از یک جمعیت 100000 نفری تعریف میشوند.
بر اساس این تعریف، سرطان های نادر به سرطان هایی با شیوع کمتر از 6/100000 نفر در سال شناخته می شوند.
باید به خاطر داشت که مطالعه سرطانهای نادر به انواع بافتشناسی نادر محدود نمیشود، بلکه شامل زیرگروههایی نیز میشود که مطالعه آنها در سرطانهای رایج (مانند سرطان پستان T4N0) دشوار است.
برعکس، سرطانهای نادر میتوانند قسمتهای نادری از سرطانهای رایج باشند که در میزبانهای غیرمعمول مانند سرطان سینه مردانه وجود دارند. فهرستی از سرطان های نادر در بزرگسالان قبلاً منتشر شده است.
مطالعات اپیدمیولوژی
بیشتر مطالعات نادر اپیدمیولوژی سرطان شامل افرادی است که در اروپا ، آمریکای شمالی ، استرالیا ، ژاپن ، ایتالیا ، ترکیه و غیره زندگی می کنند که بخش کوچکی از جمعیت جهان را تشکیل می دهند.
توصیف قطعی چنین داده هایی از کشورهای دیگر عمدتاً به دلیل عدم قطعیت در تعریف سرطان های نادر هنوز محدود است.
مؤسسه ملی بهداشت (NIH) توضیح داده است که زیرتایپ کردن در یک بیماری نادر نیز می تواند نادر در نظر گرفته شود.
با این توصیف، در مقایسه با سرطان های دوران کودکی، سرطان های اپیتلیال مکرر که در بزرگسالان تشخیص داده می شوند، به عنوان یک بیماری “نادر” در نظر گرفته می شوند.
سرطانهایی مانند کارسینوم سلولهای کبدی یا بدخیمیهای تخمدان نیز نادر هستند.
از آنجایی که مجموع موارد کمتر از 40000 در سال است، یک بروز نادر در نظر گرفته می شود. ارزیابی می شود که سرطان های زنان در سراسر جهان حدود 19 درصد از سرطان ها را در زنان تشکیل می دهند.
این تعداد نسبتاً زیاد بیشتر به دلیل شیوع بالای سرطان دهانه رحم در کشورهای در حال توسعه، به ویژه در هند است. از سوی دیگر، در بریتانیا، بدخیمیهای رحم و تخمدان به ترتیب تنها 5 و 4 درصد از سرطانهای زنان را تشکیل میدهند.
انواع سرطان های نادر
سرطانهای سلولهای زایا، تروفوبلاستیک حاملگی و نئوپلاسمهای استرومایی تخمدان کمتر شایع هستند، اما به عنوان یک گروه، نئوپلاسمهای نادر زنان نسبتاً شایع هستند.
تا همین اواخر، سه نوع شایع سرطان های زنان (تخمدان اپیتلیال، دهانه رحم و رحم) به عنوان موجودات منفرد با تغییرات اندکی برای زیرگروه بافت شناسی در نظر گرفته شده اند.
اصطلاح “تومور نادر” بیشتر برای تومورهای غیر اپیتلیال اختصاص داشت.
با این حال، الگوهای رفتاری پاتولوژیک متمایز برای زیرگروههای بافتشناسی اپیتلیال سرطانهای تخمدان، آندومتر و دهانه رحم وجود دارد که بسیاری از این نئوپلاسمها را در یک گروه نادر قرار میدهند.
به طور کلی، تومورهای نادر زنان بیش از 50 درصد از کل تومورهای زنان را شامل می شود، با حدود 80000 مورد جدید سالانه در اروپا، شامل بیش از 30 تشخیص مختلف بافت شناسی، با تعداد بسیار محدودی از بیماران در هر دسته تشخیصی.
تفاوت اقلیم و تغذیه بر سرطان های نادر
طبق دادههای ثبت شده سرطان دهلی (DCR)31، تقریباً 60.9 درصد از مردان و 46.4 درصد از زنان در دسته سرطانهای نادر قرار میگیرند.
به همین ترتیب، با توجه به تعریف IRCI، دادههای DCR سرطانهای نادر را به ترتیب در 19.4 و 23.0 درصد مرد و زن نشان داد.
شیوع برخی از انواع سرطان ها در هند و نادر بودن آنها در کشورهای غربی ممکن است به دلیل تنوع زیاد رژیم غذایی، جغرافیا، شیوه زندگی و قرار گرفتن در معرض محیطی و همچنین تنوع ژنتیکی در بین افراد باشد.
در نتیجه تنوع در بروز و نوع سرطان های نادر در نقاط مختلف جهان، علت بسیاری از این بدخیمی ها هنوز مبهم است.
سرطان های نادر دوران کودکی
برخلاف بزرگسالان، سرطان دوران کودکی به ندرت دیده می شود.
در نتیجه بهبود بقا، نرخ مرگ و میر ناشی از سرطان در کودکان در سراسر جهان کاهش یافته است.
با این حال، در دوران کودکی و نوجوانی، طیف گسترده ای از سرطان های نادر می تواند ایجاد شود.
با ویژگی های بیولوژیکی و بالینی خاص، اگرچه تغییرات زیادی بین جمعیت ها برای برخی از انواع تومورهای خاص دیده می شود.
سرطان های نادر در کودکان کمتر از 1 در 30 تومور دوران کودکی را تشکیل می دهند.
سرطان های نادر هماتولوژیک
به طور کلی، بدخیمیهای نادر هماتولوژیک، حتی در مراکز پیشرو انکولوژی که معمولاً این نوع بیماریها به آنها ارجاع داده میشود، معضل عمل پزشکی و تجربه درمان هستند.
در گذشته، تشخیص بسیاری از بدخیمیهای نادر هماتولوژیک اغلب تشخیصهای استثنایی بود. در حال حاضر، در نتیجه انحراف مولکولی شناسایی شده در این اختلالات، با اطمینان بیشتری ساخته شده است.
این پیشرفت تأثیر عمده ای بر طبقه بندی تومورها، رویکرد تفسیری و در طراحی سیاست های تحقیقاتی در این بیماری ها داشته است. پیشرفت عمده در درک پاتوژنز اختلالات میلوپرولیفراتیو بود.
افشای مبنای مولکولی برای چنین بیماری هایی به نوبه خود منجر به توسعه سیستم های طبقه بندی نیمه مولکولی برای گروه بندی بیماران بر اساس تغییرات ژنتیکی مکرر شده است.
تماشای اینکه چگونه مطالعات ژنتیک مولکولی اخیر با استانداردهای هیستوپاتولوژیک مرسوم در تنظیم یک نقشه راه عملی برای پزشکانی که از بیماران مبتلا به این بیماری ها مراقبت می کنند، ادغام می شوند، کنجکاو خواهد بود.
کارآزمایی های بالینی تصادفی شده در سرطان نادر
درمانهای معمولی که برای سرطانهای شایع و نادرانجام میشود شامل جراحی، شیمیدرمانی، رادیوتراپی و اغلب ترکیبی چند رشتهای از این درمانها است.
الگوی سنتی این درمانها هدف قرار دادن و از بین بردن سلولهای سرطانی با تداخل در رشد و بقای سلولهای تومور است.
سیستم ایمنی نقش کلیدی در سرکوب و ترویج سرطان ها با درگیر شدن در تمام جنبه های پاسخ به سرطان ایفا می کند:
- حذف سلول های سرطانی،
- حفظ تعادل بین سلول های تومور و سلول های ایمنی،
- تسهیل رشد.
افزایش درک سیستم ایمنی ما و شناسایی نئوآنتی ژن ها توجه را به شناسایی و توسعه استراتژی هایی برای تقویت پاسخ های ایمنی در جهت حذف این سلول های سرطانی و فعال سازی مجدد پاسخ های ضد تومور با کمک سلول های حافظه در صورت بروز سرطان جلب کرده است.
ایمونوتراپی
به طور خلاصه، کاربرد بالینی و کاربرد ایمونوتراپی برای سرطانهای نادر در سالهای اخیر با بهبود قابل توجهی در نتایج سرطانهای خاص (کارسینومای سلول مرکل و مزوتلیومای پلور/پریتونئال) مخلوط شده است.
بیولوژی و ریزمحیط و همچنین ناهمگونی عروق تومور در میان انواع متمایز تومورها ممکن است تفاوتهایی را در پاسخ در میان تومورهای جامد ایجاد کند.
مطالعات در حال انجام و آتی که ایمونوتراپی را با سایر روشهای درمانی ترکیب میکنند (از جمله کارآزماییهای بالینی فهرستشده در این بخش) ممکن است به گزینهای معتبر برای بیماران مقاوم به درمان با سرطانهای نادر تبدیل شوند.
ماکروفاژ درمانی
در سالهای اخیر، شکل جدیدی از ایمونوتراپی برای هدف قرار دادن و تعدیل ماکروفاژها مورد بررسی قرار گرفته است.
ماکروفاژها برای بافت میزبان خود تخصصی هستند و عملکردهای مختلفی از جمله بلع و تجزیه سلول های مرده و باقی مانده ها، حذف پاتوژن ها و تنظیم پاسخ های التهابی را انجام می دهند.
به طور سنتی، دو دسته از ماکروفاژها وجود دارد، ماکروفاژهای فعال کلاسیک (M1) و ماکروفاژهای فعال جایگزین (M2).
ماکروفاژهای M1 با ترشح سیتوکینهایی مانند TNFα، IL1-B و IL12 پاسخهای التهابی را تقویت میکنند تا جذب سلولهای Th1 T به محل التهاب را افزایش دهند.
علاوه بر این، آنها ژنها و سایر مولکولهای همتحریکی را تنظیم میکنند که پاسخ(های) سلول T را افزایش میدهند، که نقش مهمی در ضد تومور دارند.
از سوی دیگر، ماکروفاژهای M2 در عملکرد طبیعی ایمنی و هموستاز، مانند تحریک سلولهای Th2، حذف انگلها، بهبود زخم، تنظیم ایمنی و بازسازی بافت و همچنین حفظ ریزمحیط تومور (TME) نقش دارند.
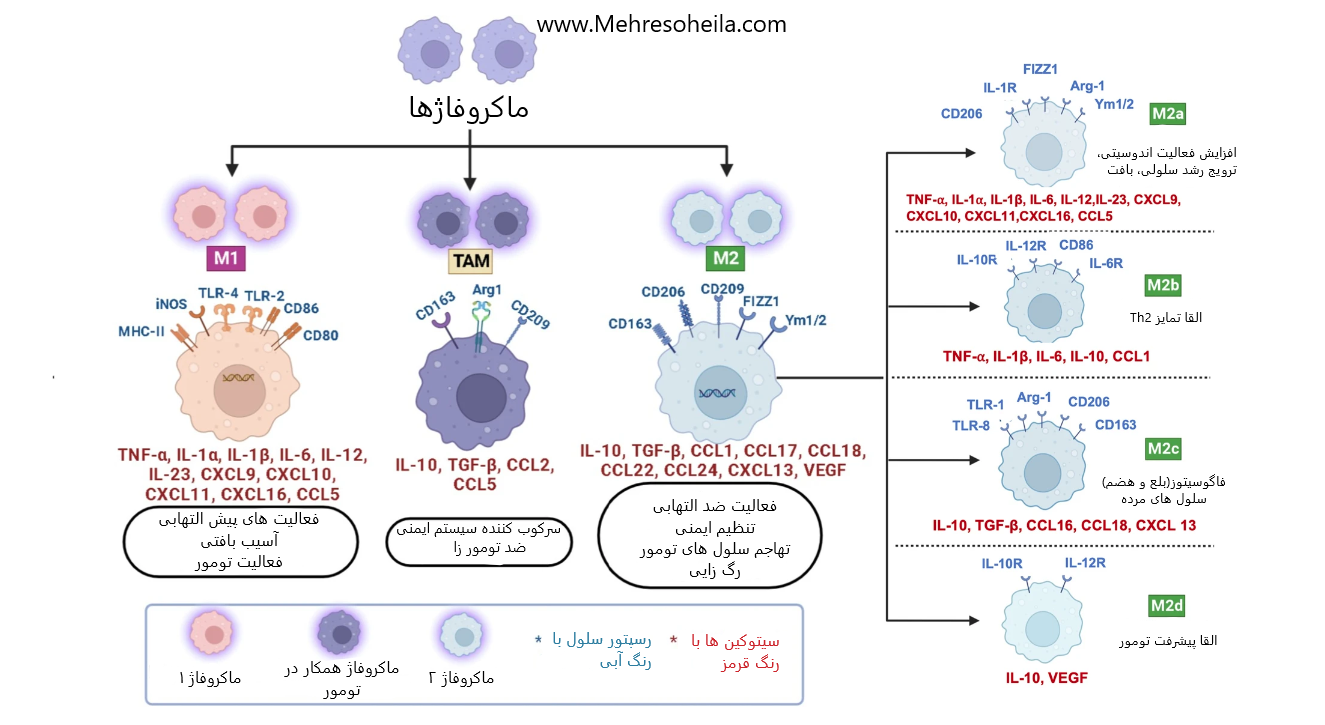
نقش ماکروفاژها در رشد و پیشرفت تومور ماکروفاژها در چندین فرآیند مرتبط با رشد و پیشرفت تومور از جمله التهاب، تنظیم ایمنی، رگزایی، تهاجم و متاستاز در ریزمحیط تومور جامد نقش دارند. هر زیرگروه ماکروفاژ با بیان سیتوکینها، کموکاینها و گیرندههای شبه تلفات مشخص میشود.
نتیجه گیری
مکانیسم های چندگانه عمل و مقاومت در پشت استراتژی های مختلف درمانی مبتنی بر ایمنی کشف می شود، درمان های ایمنی ممکن است شخصی تر شوند.
جزئیات مکانیکی که برای این استراتژیها توصیف میشوند احتمالاً به توسعه عوامل درمانی بهبودیافته و استراتژیهایی کمک میکنند که بر کاستیهای رویکردهای فعلی غلبه کنند.
درمان های ترکیبی با ایمنی درمانی احتمالاً در آینده به رشد خود ادامه خواهند داد.
برای سرطانهای نادر، یکی از روشهای درمان ترکیبی، تجویز دو نوع درمان مشابه، به عنوان مثال دو مهارکننده نقطه بازرسی ایمنی است.
برخی از کارآزماییهای بالینی تکمیلشده و برخی از آزمایشهای در حال انجام، افزایش کارایی را در درمان تومورها با این رویکرد گزارش کردهاند.
یکی دیگر از رویکردهای ترکیبی، افزودن یک نوع ایمونوتراپی به درمانهای مرسوم یا ترکیب چندین اشکال ایمنی درمانی با هم است.